 (一)骨質疏鬆常見轉介議題與Choosing Wisely議題
(一)骨質疏鬆常見轉介議題與Choosing Wisely議題
講者:臺大院老年醫學部 詹鼎正主任
骨質疏鬆症流行病學
 骨質疏鬆症(osteoporosis)即骨骼密度減弱或骨頭品質變差,增加骨折的風險。原則上骨折發生前無症狀,惟藉由骨密度(bone mineral density, BMD)測定,其中以雙能量X光吸收儀(dual-energy X-ray absorptiometry, DXA)為黃金標準,可精確量測,應測量腰椎、髖骨,兩者都做更好,若兩處都因骨折而不能測定時,則可用非慣用側前臂橈骨 1/3 處之測定取代。其檢測以T值(標準差)作為指標,T值介於-1.0及-2.5為低骨量(osteopenia);T值≤ -2.5為骨質疏鬆症。若為嚴重性骨質疏鬆症(severe osteoporosis)合併骨折,治療可申請健保藥物給付。病人發生一次骨折後,再發生率約為50%,髖部骨折女性發生率大致為男性兩倍,但男性死亡率高於女性,且髖部骨折易導致失能,需他人照護。即便如此,髖部骨折發生後,不到30%的病人有實際接受藥物治療,治療率很低。
骨質疏鬆症(osteoporosis)即骨骼密度減弱或骨頭品質變差,增加骨折的風險。原則上骨折發生前無症狀,惟藉由骨密度(bone mineral density, BMD)測定,其中以雙能量X光吸收儀(dual-energy X-ray absorptiometry, DXA)為黃金標準,可精確量測,應測量腰椎、髖骨,兩者都做更好,若兩處都因骨折而不能測定時,則可用非慣用側前臂橈骨 1/3 處之測定取代。其檢測以T值(標準差)作為指標,T值介於-1.0及-2.5為低骨量(osteopenia);T值≤ -2.5為骨質疏鬆症。若為嚴重性骨質疏鬆症(severe osteoporosis)合併骨折,治療可申請健保藥物給付。病人發生一次骨折後,再發生率約為50%,髖部骨折女性發生率大致為男性兩倍,但男性死亡率高於女性,且髖部骨折易導致失能,需他人照護。即便如此,髖部骨折發生後,不到30%的病人有實際接受藥物治療,治療率很低。
骨質疏鬆症常見評估工具有FRAX®骨折風險評估,可自行上網搜尋,若主要骨鬆症骨折風險大於20%及髖部骨折大於3%者,建議就醫。臺灣人骨質疏鬆症自我評量表(Osteoporosis Self-assessment tool for Taiwanese, OSTAi),若OSTAi ≧2為高度風險,即罹患骨質疏鬆症機率為60%以上。極高骨折風險評估(2020 AACE recommendation),若病人符合其中一項應更積極治療。骨質疏鬆風險測試(Internation osteoporesis foundation, IOF),可自行上網搜尋。綜合上述,若為高風險與極高風險的病人至醫療院所評估與治療(如圖1)。
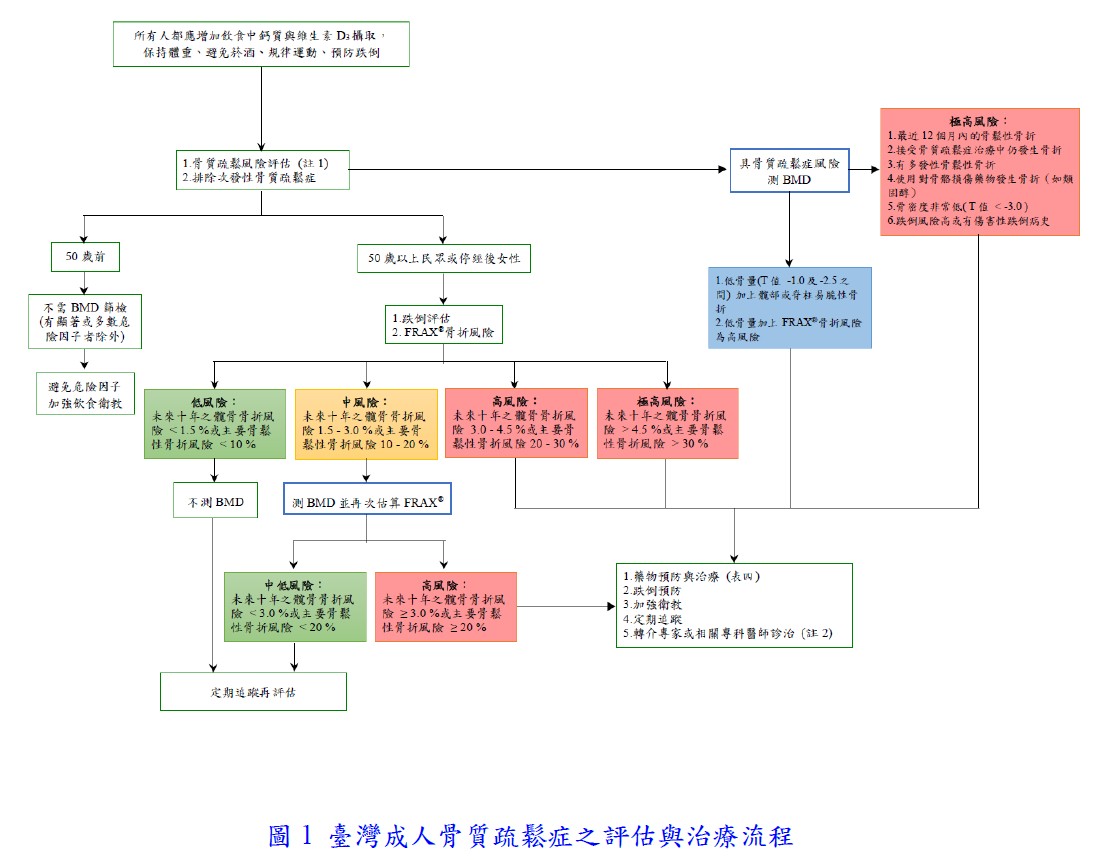
骨質疏鬆症的主要臨床風險因子:年齡、性別、低身體質量指數(BMI)、骨折(特別是髖部、脊、椎骨、腕部骨折)、身高減少(超過4公分)、夫母髖部骨折史、目前抽菸、飲酒過量、次發性骨質疏鬆症、藥物、長期臥床、衰弱症或缺少運動、跌倒等。
中華民國骨質疏鬆症學會建議接受骨密度檢查者,包括:65歲以上婦女或70歲以上男性、65歲以下具有危險因子的停經婦女、50~70歲具有骨折高風險因子的男性等。然而,Choosing Wisely (American academy of family physicians, AAFP)建議65歲以下婦女,與低骨折風險男性不需要進行骨密度檢查,這與學會一致。
骨折聯合照護服務(Fracture Liaison Service, FLS)為對於已發生骨鬆骨折的病人提供的聯合照護體系,包括各領域專業人員及個案管理師,依世界骨鬆基金會最佳執業藍圖十三項指標評值成效,以提升病人的檢查率及治療成效,降低骨折率及死亡率。至目前為止,全國已建立35處骨折聯合照護服務,並於2017、2019年獲得IOF頒發全球最佳相關獎項。以臺大醫院總院骨折聯合照護服務為例,針對50歲以上新發現的骨折病人,服務流程如圖2。
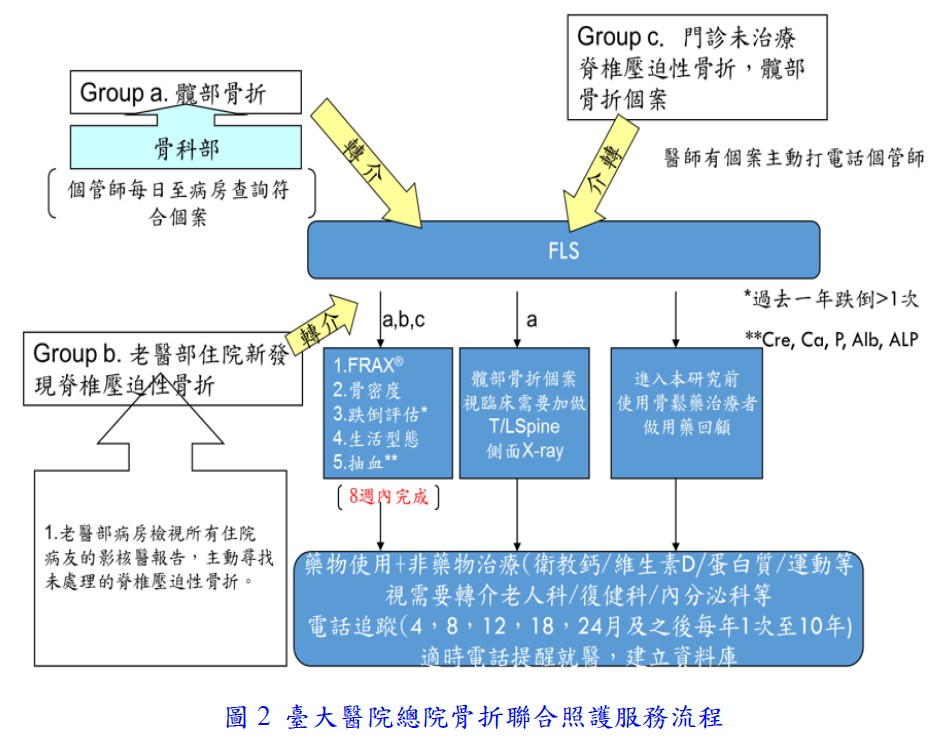
骨質疏鬆症預防與治療
1. 預防:提高巔峰骨量,減少骨質流失,與預防跌倒,避免骨折。
2. 非藥物介入:改善日常生活行為,戒菸和戒酒,去除危險因子;足量鈣和維生素D3攝取;荷重運動、肌力增強運動和平衡訓練;改善居家和公共環境,使用防範措施,防範骨折。
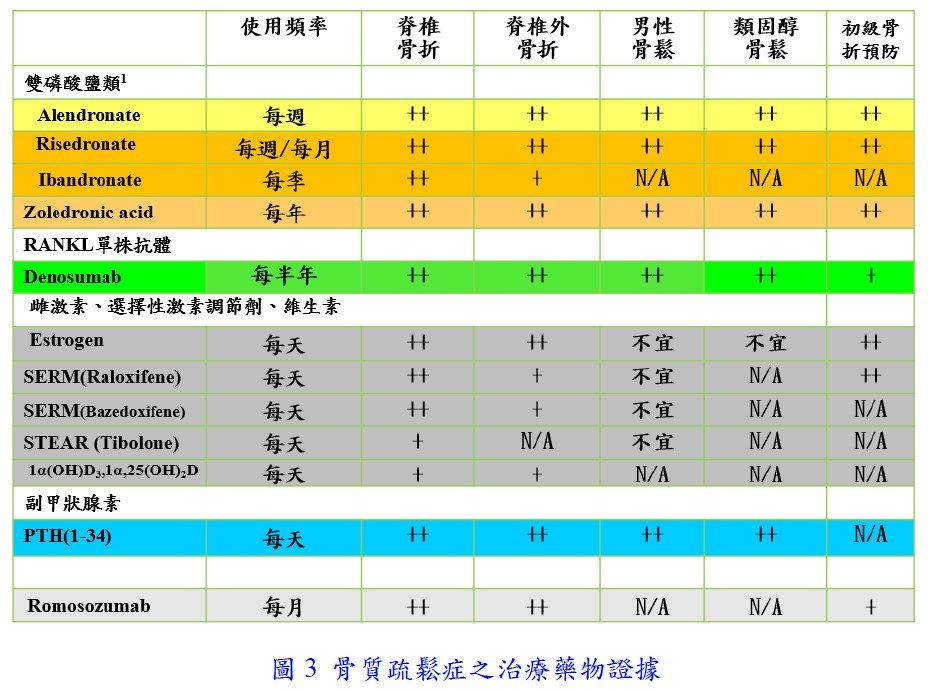
3. 藥物追蹤及治療:使用造骨刺激藥物,SERM、雌激素、dMab、abaloparatide、romosozumab、teriparatide等,停止治療後,骨量會有快速流失,須銜接其他抗骨吸收類藥物,以避免多發性骨折風險發生。唯有雙磷酸鹽有用藥假期(drug holiday),因雙磷酸鹽會留在體內慢慢釋放,維持骨密度。一般而言,注射劑型三年,口服劑五年可進行評估,如果骨密度改善良好,骨折風險低,可考放假,之後定期追蹤,風險提升時再用藥。骨折高危險或極高風險患者病患仍可建議繼續用藥,口服劑可繼續延長5年治療(共6至10年),注射劑型持續6年治療後再評估是否繼續治療。詳見圖3。另外,使用骨鬆藥物前應檢查血鈣、磷及腎功能,用藥治療需一年以上(最好持續三年),累積藥量若不及一半是沒有骨折防治效果。
評估治療成效,建議一年以上,最好兩年測量再追蹤骨密度,因骨密度改變超過最小顯著差異值(LSC)始可認為有顯著變化(髖骨3~6%或腰椎2~4%以上);對於未接受治療者不建議一年之內重覆測量,除非使用類固醇前後6個月的病人(Glucocorticoid-induced Osteoporosis, GIOP)。
骨質疏鬆症轉介
高風險患者建議透過雙向轉診系統進行相關檢查及治療。院所轉介病人到本院進行DXA檢查,院所可開立骨鬆治療藥物,將回覆院所DXA檢查及胸腰椎側面X光片報告。若院所無法開立骨鬆治療藥物,本院會接手骨質疏鬆症治療,並將其餘的慢性病將轉回原院所繼續追蹤。作者感謝中華民國骨質疏鬆症學會授權相關圖表內容。
院所提問
Q1:請問T score的分數與未來發生骨折的機會(N年內)是否有研究數據可參?
A1:T score每多一個標準差(-1),風險增加兩倍。
Q2:請教關於T值的認定,在健保抽審時和審查委員有歧見!可否依學會的成人骨鬆指引為做為健保治療的準則,謝謝!
A2:學會的指引與健保給付標準內容不盡相同,健保抽審可能還是要回歸健保給付標準。
Q3:骨鬆藥是吃ㄧ輩子,雙磷酸鹽又是會存在骨內,那要拔牙時有什麼要注意事項?
A3:請見牙科楊湘醫師下頁專文介紹。
骨質疏鬆症藥物治療的牙科評估注意事項與建議(會後補充)
臺大醫院 牙科部 楊湘醫師
 自2003年一些臨床醫師及學者開始注意到使用雙磷酸鹽類藥物後的病人發生顎骨壞死的情形,並有關於雙磷酸鹽類藥物相關顎骨壞死(bisphosphonate-related osteonecrosis of the jaw, BRONJ)的案例報告,但後續又有學者發現不僅是雙磷酸鹽類藥物,其他抗骨吸收藥物如單株抗體藥物(Denosumab)及抗血管生成藥物等,亦可能發生顎骨壞死的情形,所以美國口腔顎面外科醫學會(American Association of Oral and Maxillofacial Surgeons, AAOMS)於2014年更名為藥物相關顎骨壞死(medication-related osteonecrosis of the jaw, MRONJ)。
自2003年一些臨床醫師及學者開始注意到使用雙磷酸鹽類藥物後的病人發生顎骨壞死的情形,並有關於雙磷酸鹽類藥物相關顎骨壞死(bisphosphonate-related osteonecrosis of the jaw, BRONJ)的案例報告,但後續又有學者發現不僅是雙磷酸鹽類藥物,其他抗骨吸收藥物如單株抗體藥物(Denosumab)及抗血管生成藥物等,亦可能發生顎骨壞死的情形,所以美國口腔顎面外科醫學會(American Association of Oral and Maxillofacial Surgeons, AAOMS)於2014年更名為藥物相關顎骨壞死(medication-related osteonecrosis of the jaw, MRONJ)。
藥物相關顎骨壞死指的是曾經或正在使用抗骨吸收或抗血管生成藥物的不良反應,因而引起上顎或下顎顎骨漸進式破壞及凋亡,造成顎骨曝露或於顎顏面區出現口內或口外廔管超過八星期以上,且病人不曾接受過頭頸部放射線治療。症狀包括非齒源性牙齒疼痛、顎骨或鼻竇疼痛、口內或口外化膿腫脹、顏面感覺異常等。
雙磷酸鹽類藥物常用於治療骨質疏鬆症以預防骨折發生,或處理癌症病人如乳癌、肺癌、攝護腺癌的骨轉移問題及多發性骨髓瘤的相關骨骼症狀,於2010年上市的單株抗體藥物也有類似療效,但作用機轉不一樣,二類藥物均可抑制噬骨細胞的作用,阻止骨骼重塑(bone remodeling)功能,差異在於雙磷酸鹽類藥物的半衰期很長且會長期存留於骨骼中,而單株抗體藥物的半衰期短且不會結合到骨頭上,在施打後的六個月內療效會逐漸消失。
癌症病人使用抗骨吸收藥物發生顎骨壞死的風險機率較高,總括而言約略小於5%,文獻回顧則因追蹤時間不等,使用Zoledronate從0到 18%皆有,是使用安慰劑病人的2-8倍風險;使用Denosumab的風險則是從0到 6.9%。而在骨質疏鬆症病人的總括風險機率則小於0.05%,使用Zoledronate和口服雙磷酸鹽類藥物分別為小於等於0.02%和0.05%,使用Denosumab的風險則為0.3%,最新的藥物Romosozumab為0.03-0.05%,但仍需持續觀察。早期的文獻提出骨質疏鬆症病人使用雙磷酸鹽類藥物的期間長短風險會從接近零到使用四年以上陡升到0.21%,但最近的實證報告長達九年的雙磷酸鹽類藥物使用發生顎骨壞死的風險則和安慰劑組無顯著差別。因此可知骨質疏鬆病人使用抗骨吸收藥物雖然有發生顎骨壞死的風險,但是非常低,毋須因此而忌諱使用藥物。
其他如合併服用類固醇、免疫調節劑或抗血管生成藥物,貧血或糖尿病的共病等也會增加骨質疏鬆症病人發生顎骨壞死的風險,至於菸草是否增加風險則未有定論。
牙科的齒槽骨手術尤其是拔牙,在傷口癒合過程中因涉及骨骼重塑的機轉,無疑是引發藥物相關顎骨壞死的最主要因素,約佔62-82%。骨質疏鬆症病人使用雙磷酸鹽類藥物及單株抗體藥物後因拔牙而發生顎骨壞死的風險分別為0-0.15%和1%。如果牙齒在被拔除前合併有牙周或牙根尖發炎或感染時,則更會增加顎骨壞死風險。至於其他牙周或根尖手術的風險則未知,使用單株抗體藥物後進行人工植牙的風險為0.5%。75%的顎骨壞死發生在下顎,25%發生在上顎,4.5%同時發生在上下顎。
骨質疏鬆症病人在開始使用抗骨吸收藥物前,應告知病人用藥後有可能發生藥物相關顎骨壞死的風險,及維持口腔衛生的重要性,並建議先行照會牙科醫師,進行完整的口腔及牙科X光片檢查,先行將無法留存重建的牙齒拔除,待傷口癒合後再進行用藥,若配戴活動假牙則須留意是否有良好的密貼及固持性,不會磨傷顎骨黏膜。用藥期間及以後均須維持良好的口腔衛生,定期至少每半年一次的牙科回診,並請病人主動告知牙醫師目前或曾經使用的抗骨吸收藥物的種類、頻率及使用期間,以期能及早發現病灶並進行風險評估以提供適切治療。
以往文獻建議可使用骨骼代謝指標(bone turnover biomarker)來進行用藥後的顎骨壞死風險評估,但目前未被證實是有效評估工具。
用藥後若需進行齒槽骨手術如拔牙或人工植牙時,曾有學者提出暫停使用抗骨吸收藥物(drug holiday)的建議,但至今仍是未有定論,文獻報告的結論並不一致,所以無法有確切的建議,可能須依個案實際相關風險因子進行評估。倒是有研究報告指出使用單株抗體藥物的病人在停藥後,反而會反彈性增加骨吸收而造成脊椎骨折,權衡之下,建議在最後一次用藥後的三至四個月當單株抗體藥物抑制噬骨效力減弱時可執行拔牙,然後在6-8星期後便可再持續用藥。
藥物相關顎骨壞死大多發生於使用藥物的癌症病人,於骨質疏鬆症病人的風險雖然存在但相對而言很低,經由跨科別的合作及共同照護,並採取預防措施可降低風險,而良好的口腔衛生一定是擁有良好生活品質的不二法門。
參考文獻
Ruggiero SL, Dodson TB, Aghaloo T, Carlson ER, Ward BB, Kademani D.
American Association of Oral and Maxillofacial Surgeons’ Position Paper on Medication-Related Osteonecrosis of the Jaws—2022 Update
J Oral Maxillofac Surg. 2022 May;80(5):920-943. doi: 10.1016/j.joms.2022.02.008. Epub 2022 Feb 21. PMID: 35300956


