
癌症疼痛的進階治療
癌症止痛的一般原則
疼痛是癌症病患最常見的症狀之一,對癌症病患生活品質影響甚鉅,患者不但要和死亡的恐懼搏鬥,還得飽受癌症疼痛所造成之生理心理的折磨。隨著醫療技術的進步,癌症病人存活期越來越長,臨床上要同時處理病人頑固性癌症疼痛的機率也越來越高。癌症病人的疼痛原因可能來自腫瘤本身對身體組織的浸潤破壞,例如骨轉移之病理性骨折所引起的疼痛;或是治療過程所引起,如化療放療引起的黏膜發炎等等。以疼痛程度而言,一般我們會用所謂的疼痛分數做為評估,疼痛分為0到10分,0分是完全不痛,1-3分為輕度疼痛,4-6分為中度疼痛,7-10為嚴重疼痛。依照世界衛生組織的止痛建議,不同程度的疼痛各有不同處理原則。輕度疼痛可以使用非類固醇消炎止痛藥(NSAID)或普拿疼,中度疼痛則採用弱效類鴉片如codeine、tramadol等,至於重度疼痛就應使用強效類鴉片製劑如fentanyl經皮貼片或嗎啡。原則上以口服或經皮等非侵入性投藥方式給予,若情況需要,也可以靜脈注射止痛藥達到更快速的止痛效果。依上述原則,輔以適當佐劑(Adjuvant drugs),80-90%癌症疼痛可以得到控制,但是鴉片類藥物會伴有噁心、嘔吐、昏昏欲睡、皮膚癢、小便不順等副作用,嚴重時甚至會抑制呼吸或造成意識不清。在病人接受規律的止痛治療一段時間後,還可能產生藥物耐受性(Tolerance),也就是止痛效力減弱而需增加劑量的狀況。
頑固性癌痛的定義與治療方式
即使經過類鴉片藥物調整轉換及止痛佐劑的使用,臨床上仍有10-20%的癌症疼痛無法以口服或經皮藥物達到止痛效果,或對藥物產生難以忍受的副作用,也就是所謂的頑固性癌痛。針對這一群病人,我們需要進行侵入性的進階止痛療法。進階止痛療法在概念上可分為兩大類,第一類是針對疼痛的訊息從周邊組織傳遞到大腦的路徑進行阻斷或破壞,也就是一般我們所謂的神經阻斷(Nerve block)或神經破壞術(Neuroablative procedure);另一大類則是將鴉片類藥物直接遞送到脊椎腔內以避免全身性藥物投予所造成的副作用,也就是脊椎內給藥系統(Intraspinal drug delivery system)。以下將介紹常用的神經破壞術及脊椎內幫浦在頑固性癌症疼痛的應用。
神經破壞術處置簡介
在開始介紹神經破壞術處置之前,必須釐清幾個觀念:
- 癌症止痛所使用的神經阻斷精確來說是一種神經破壞術,是利用藥物(如純酒精或苯酚)或射頻電燒(radiofrequency ablation)永久性的將目標神經破壞,是不可逆的處置。與我們一般所指利用局部麻醉藥物做暫時性的麻醉阻斷是不一樣的。
- 神經破壞術並非亂槍打鳥,必須有適當的標的方能進行,例如胰臟癌引發的腹部內臟疼痛我們可以藉由破壞內臟神經(splanchnic plexus,這是支配腹部臟器感覺的交感神經叢)而止痛。然而針對脊髓本體甚至腦幹或大腦破壞的技術例如cordotomy,hypophysectomy雖然在神經生理上似乎有其合理性,然而在臨床上卻早已被證明效果不彰且破壞性太大而很少被使用。
- 常用之神經破壞術範圍皆在主動脈、上下腔靜脈或脊椎周邊,有一定程度的併發症風險。因此所有進行神經破壞術的病患都應審慎評估其預計存活期、風險與效益。
- 所有的神經破壞術可視為影像導引的微創手術,希望能以最小的破壞範圍達到最顯著的止痛效果。針對常規於開刀房內進行的神經破壞術我們都會以螢光透視鏡輔以超音波的雙重影像導引進行。同時我們也會以神經刺激器輔助定位神經,避免傷害重要的運動神經。其基本配置如圖1。
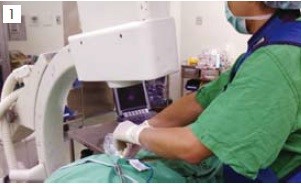
- 神經破壞術不是止痛萬靈丹,並非接受過神經破壞術就不再需要止痛藥物,應被視為一種輔助性的止痛療法,其效果亦有其侷限性。以胰臟癌所進行的內臟神經阻斷為例,我們僅破壞支配上腹部內臟感覺(visceral sensation)的交感神經叢,對於胰臟癌所引起的悶痛或脹痛有很好的效果。然而若腫瘤有合併有腹壁的侵犯,這種疼痛則屬於體節痛(somatic pain)的範疇,單純內臟神經阻斷並不能緩解體節痛而必須使用止痛藥或進行體節神經破壞。另外神經阻斷的止痛效果亦非一勞永逸,隨著病患病情的惡化,神經可塑性的變化(Neuroplasticity change)以及小部份的神經再生,疼痛都有可能再度出現或惡化。更常見的是原本最顯著的疼痛病灶被緩解了之後,原本次要的疼痛就會變成新的關注焦點,產生新的疼痛。
以下簡單介紹胸腔與腹腔腫瘤引發之頑固型疼痛所進行之神經阻斷。
胸腔神經阻斷
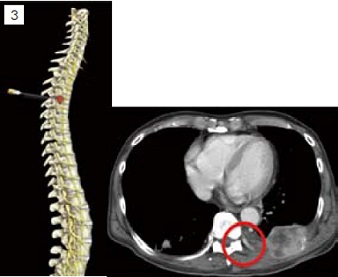
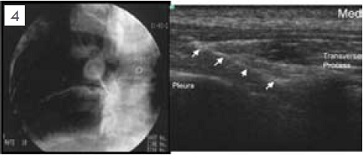
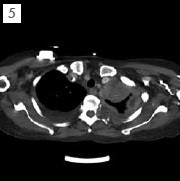
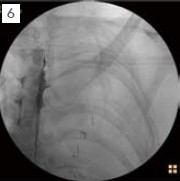
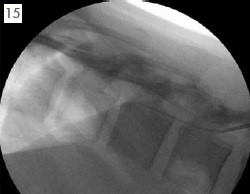
當腫瘤合併肋膜轉移或肋骨轉移(如圖2)。病患會出現所謂的胸腔症候群(Chestwall syndrome),這是一種體節性與內臟性的混和疼痛,病患可能會抱怨如帶狀泡疹般繞身體半圈的疼痛或燒灼感,有些病患則可能會伴隨著每一次的呼吸與咳嗽都有著牽扯撕裂的感覺。當藥物止痛效果不佳時可考慮進行肋間神經阻斷(Intercostal nerve block)將掌管此一區域的一條至數條肋間神經破壞掉來止痛。由於肋間神經之下就是肋膜,因此肋間神經阻斷有非常高比率的氣胸併發症。目前我們採取影像導引傍脊椎神經叢破壞(Paravertebral neurolysis),我們在超音波與螢光透視鏡的導引下,將神經阻斷針導引到傍脊椎空間(Paravertebral space)如圖3所標示範圍,然後注射高濃度酒精或苯酚將肋間神經與交感神經鍊同時破壞,期望能同時阻斷體節性與內臟性的疼痛。由於我們同時採用的超音波與螢光透視兩種影像導引(如圖4)不但可以大幅增加精確性更可以有效避免氣胸的產生。然而有部分的病患其病灶太過靠近脊椎或有明顯的神經孔侵犯,如下之斷層掃描顯示病灶已侵犯脊椎骨本體並壓迫肋間神經的出口處(如圖5)。針對這樣的病患我們則會嘗試採取硬膜外酒精注射來進行神經破壞,如圖6。在螢光透視鏡監視下將硬膜外導管置放到患側的硬膜外腔,在注射顯影劑確認藥物擴散範圍可涵蓋疼痛最劇烈的區域後再進行高濃度酒精注射破壞腫瘤侵犯區域的背根神經節(Dorsal root ganglia)。
.jpg)
腹腔神經叢阻斷
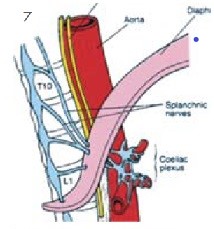
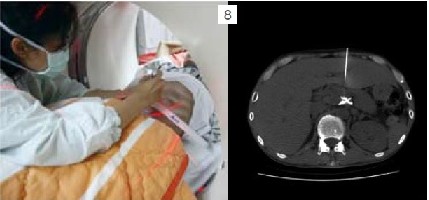
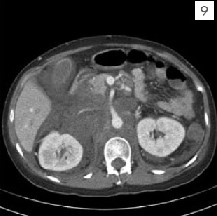
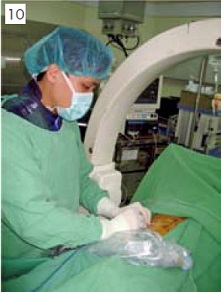
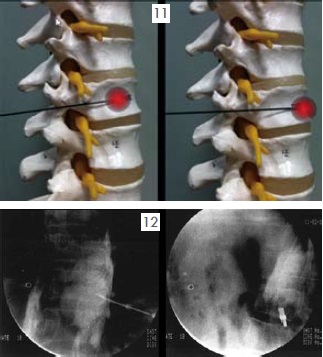
這是目前最常使用的神經阻斷術,也是實證醫學上最有效可以改善癌末病患生活品質的處置之一。支配上腹部器官的內臟感覺神經藉由兩側T5至T12的交感神經將內臟疼痛的感覺傳遞至脊髓。其中T5-T9匯聚成大內臟神經(Greater splanchnic nerve)、T10-T11形成小內臟神經(Lesser splanchnic nerve)、T12則單獨形成最小內臟神經(Leasts planchnic nerve)。這錯縱複雜的內臟神經叢穿過橫膈膜後在主動脈與celiac trunk周邊形成celiac plexus,其神經元本體則形成celiacganglion。如圖7。傳統上針對源自上腹部器官的頑固性腹痛,包括胃癌、胰臟癌、肝癌、膽管癌或轉移性病灶造成之肝轉移、主動脈旁淋巴結轉移與癌性腹膜炎所引發的內臟疼痛可以用celiac plexus block止痛,將高濃度酒精藉由影像導引注射在主動脈前方。如圖8中以斷層掃描導引進行腹腔神經叢阻斷。然而由於腫瘤的侵犯會讓解剖構造扭曲,往往會改變神經所在的相對位置,加上主動脈前方的神經叢阻斷往往對於有主動脈旁淋巴結轉移(如圖9)所造成的深部腹痛與上腰部疼痛之止痛效果較差。因此目前我們常規採取雙側內臟神經叢阻斷(Bilateral splanchnic neurolysis)來取代腹腔神經叢阻斷。手術進行方式是病患採取趴臥姿勢(如圖10),在X光與超音波導引下將射頻電燒探頭導引至內臟神經叢所在位置(通常為T11與T12脊椎本體的側面),然後電刺激確認神經位置後給予適當麻醉,然後以射頻電燒將神經破壞(範圍如圖11),最後再注射高濃度酒精將神經叢做完全的破壞,如圖12顯影劑擴散範圍。根據統計,有80-90%的腹腔癌症病患可以得到顯著的止痛效果,此外,由於內臟神經阻斷是一種交感神經阻斷,而這群病患往往在神經阻斷前因為大量使用鴉片類藥物而有嚴重的便秘問題,在交感神經阻斷後會有輕微腹瀉的情形,算是另外一種額外的治療效果。此外針對骨盆腔腫瘤則可以Superior hypogastric plexus block;會陰部腫瘤則以Ganglion impar block作為加強止痛之處置。
脊椎內給藥系統簡介
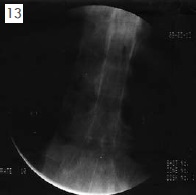
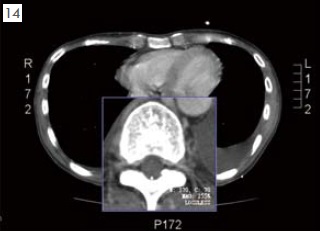
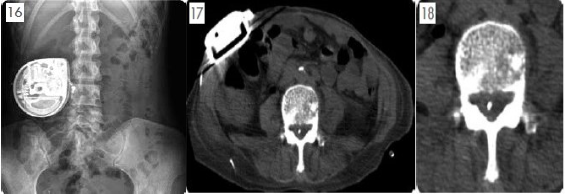
當我們給予病患口服鴉片類藥物後,不可避免的這些藥物需要經由腸胃道吸收進入血液然後輸送到鴉片類藥物的作用地點―中樞神經系統。也因此口服鴉片類藥物會合併許多的腸胃道併發症例如嚴重便秘而限制了藥物劑量的增加。藥理研究顯示靜脈給予嗎啡是口服的三倍效力,若將嗎啡遞送到硬膜外腔(Epidural space)則有口服的三十倍效力,若更進一步將嗎啡直接在脊椎腔內輸注,則有口服嗎啡的三百倍效力。脊椎內給藥更重要的好處是可以大幅降低腸胃道相關的併發症例如噁心、嘔吐、便秘等。當臨床上遇到病患因無法忍受鴉片類藥物副作用或止痛效果不良的病患即可以嘗試脊椎內給藥。在開始進行脊椎內給藥之前,我們需要評估病患的預計存活期來決定是否應植入永久性裝置。當病患預計存活期僅有三個月以內,原則上我們會安裝暫時性導管來幫助止痛,當病患預計可存活三個月以上則會考慮植入脊髓腔內嗎啡幫浦(Intrathecal morphine pump 或Intrathecal drug delivery system)。硬膜外藥物輸注: 由於脊椎腔內(Intrathecal space)並沒有免疫的保護,因此為降低中樞神經系統感染之風險,暫時性導管我們皆會在影像導引下放到疼痛最劇烈區域對應脊椎節段的硬膜外腔(Epidural space)如圖13為一胃癌病患在置放硬膜外導管後注射顯影劑可觀察到藥物可均勻地擴散到兩側並覆蓋T4至T11區域,之後我們再開始施予硬膜外嗎啡輸注。斷層掃描可觀察到導管位於硬膜外腔(如圖14)。藉由適當的藥物調整,病患可以獲得良好的止痛,原則上暫時性導管可以使用二至四週左右。脊髓腔內嗎啡幫浦( I n t r a t h e c a l morphine pump):當預計可存活大於3個月以上的頑固性癌痛病患接受短暫硬膜外嗎啡輸注(一週左右)後,若確認可以降低至少50-70%的疼痛即可考慮是否植入永久性幫浦作為長期止痛之方式。所謂脊髓腔內嗎啡輸注療法就是將一個永久性導管在影像導引下放入脊髓腔(Intrathecal space)內的適當位置(最劇烈疼痛區域所對應的脊髓位置)後(如圖15)。再將導管連接到肚皮下方所植入之約巴掌大小的微電腦幫浦,幫浦內儲存的嗎啡就可以經由導管注入至脊椎腔內。如圖16-18。術後斷層掃描可以觀察到幫浦本體位於皮下而導管位於脊髓腔內,幫浦可經體外的控制器由醫師處方設定給予病患病情需要的劑量。幫浦內儲存的嗎啡需定期更換,最長期限為180天,或依據病情需要而添加或調整。所有更換補充動作只需於病患體外進行,不用再將幫浦取出。可根據病患的疼痛狀況,隨時調整劑量自動給藥,以達到良好的止痛效果,只要定期回門診補充藥量即可,也不必擔心忘記吃藥等問題。由於止痛效果優良,脊髓腔內嗎啡輸注療法在歐美國家非常普遍,在台灣的普遍性則仍有待推廣。
結語
對於癌症病患來說,除了要和疾病搏鬥死神拔河,還要面對生理以及心理的煎熬苦痛,而許多癌症末期的患者更因為疼痛不堪所造成的負面憂鬱情緒,無法和家人好好共度生命最終的旅程。但隨著醫藥科技的進步,癌症止痛方式日趨多元,除了傳統的藥物治療外,我們更能借助影像導引的神經阻斷為病患打造客製化的止痛療法,不僅能更有效的緩解癌症疼痛,也能擁有較佳的生活品質。
【文章出處:景福醫訊 台大醫院麻醉部暨腫瘤醫學部 林至芃醫師】